|
|
|
|
|
|
|
|
|
Fotoni preveggenti
Annibale
D’Ercole
|
Nel secolo diciottesimo, la
stragrande maggioranza degli studiosi aderiva alla teoria corpuscolare della
luce di Newton, secondo cui la radiazione consiste di un aggregato di
corpuscoli piccolissimi. La contemporanea teoria ondulatoria di Huygens
poteva vantare solo pochi sostenitori. All’inizio del secolo diciannovesimo,
però, Young scoprì che in certe circostanze due fasci di luce possono
indebolirsi a vicenda, un fenomeno assolutamente inspiegabile nella teoria
corpuscolare. Il famoso esperimento di interferenza di Young confermò
inequivocabilmente la natura ondulatoria della luce. All’inizio del ventesimo
secolo, tuttavia, il fenomeno dell’effetto fotoelettrico si mostrò
refrattario a una spiegazione basata sulla teoria ondulatoria e fu
interpretato da Einstein ipotizzando una natura corpuscolare della luce. Si è
così affermato per la radiazione (ma anche per la materia) il concetto di
dualismo onda-particella. Ogni processo può essere interpretato in termini
ondulatori o corpuscolari, ma non siamo in grado di determinare la “vera”
natura della luce. Data la fondamentale importanza dell’esperimento di Young
e dell’effetto fotoelettrico nella formulazione di questo dualismo, ne
riportiamo gli aspetti salienti. L’esperimento
di Young Un fronte luminoso (che assumiamo,
per semplicità, monocromatico, ovvero composto da onde di una sola lunghezza
d’onda l, come quelle di un laser) investe
un diaframma dotato di due fenditure. Se la luce fosse composta da
particelle, esse proseguirebbero la loro traiettoria rettilinea oltre le
fenditure e andrebbero a formare due bande luminose sopra uno schermo posto
oltre il diaframma. Invece, sullo schermo compare un sistema di frange
equidistanti chiare e scure (si veda Fig.
2). Questo si spiega ammettendo che dalle aperture del diaframma si
diffondono in avanti onde sferiche in grado di interferire. Consideriamo due
percorsi luminosi r1 e r2 (indicati dalle due
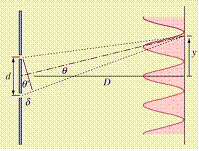
linee punteggiate in Fig. 5) che
partono dalle due fenditure e che giungono nel medesimo punto y dello schermo. Se la distanza D tra diaframma e schermo è molto
maggiore della distanza d tra le
due fenditure (D >> d), si ha q¢ » q
e la differenza di lunghezza d = r1 – r2 può
essere scritta come d = d sinq.
Fig. 5. Schema della
formazione di frange di interferenza nell’esperimento di Young. Si ottiene la
formazione di una frangia luminosa nel punto y se le ampiezze delle due onde che avanzano lungo r1 e r2 interferiscono costruttivamente in y, ovvero se la cresta (o il ventre)
di una si sovrappone alla cresta (al ventre) dell’altra. Questo avviene se d è pari a un multiplo
intero di l,
ovvero d sinq = nl,
n = 1, 2, 3, … (1) Dalla Fig. 5 si vede che tanq = y/D. Se si è posto lo
schermo a grande distanza, l’angolo q
è piccolo e vale la seguente catena di approssimazioni: tanq » sinq » q »
y/D. Dunque, in base all’eq.
(1), le frange luminose si formano nei punti yn yn »
nl D/d,
n = 1, 2, 3, … Lo schermo, invece,
rimane in ombra in tutti i punti in cui convergono due tragitti la cui
differenza in lunghezza è data da un numero semintero di lunghezze d’onda, in
modo che la cresta di un’onda si sovrapponga con il ventre dell’altra dando
luogo a un’interferenza distruttiva: d sinq = (n + 0,5)l,
n=1, 2, 3, … L’effetto
fotoelettrico Se una superficie metallica viene
illuminata con luce appropriata, è possibile estrarne elettroni. È naturale supporre
che il campo elettrico della radiazione, se sufficientemente intenso, riesca
a strappare gli elettroni dall’attrazione
dei nuclei atomici del metallo e sbalzarli via. Tuttavia, le caratteristiche
dell’effetto fotoelettrico non si riescono a spiegare all’interno di uno
schema ondulatorio della radiazione elettromagnetica. Queste caratteristiche
si riassumono nei seguenti punti: 1)
la
velocità degli elettroni (e dunque la loro energia cinetica) espulsi non
dipende dall’intensità della radiazione, ma dalla sua frequenza: maggiore è
la frequenza, maggiore è la velocità; 2)
raggi
luminosi di frequenza inferiore a una certa frequenza critica ncr (che dipende dal tipo di metallo)
non sono in grado di estrarre elettroni, indipendentemente dalla loro
intensità; 3)
il
numero degli elettroni estratti è proporzionale all’intensità luminosa: se
questa raddoppia, raddoppia anche quello. Ora, si intuisce
facilmente che l’energia trasportata da un’onda è legata alla sua ampiezza
(per la precisione, il quadrato dell’ampiezza): i danni provocati da una
mareggiata sono maggiori per onde con altezza maggiore. Analogamente, l’intensità
di un fascio luminoso (che assumiamo, per semplicità, monocromatico) dipende
dall’ampiezza dell’onda elettromagnetica, ovvero alla massima intensità
raggiunta dal campo elettrico (e magnetico) durante le oscillazioni.
Pertanto, ci si aspetta che un raggio luminoso più intenso interagisca con lo
stesso numero di elettroni, ma trasferendo loro una maggiore energia, e
portandoli quindi a velocità più alte. Come si vede, la teoria ondulatoria
della luce conduce a previsioni in disaccordo con i fatti sperimentali
elencati in precedenza. Nel 1905, Albert Einstein spiegò l’effetto
fotoelettrico con l’ipotesi che i raggi luminosi siano composti da
particelle, chiamate fotoni, la cui energia è direttamente proporzionale alla
frequenza della radiazione corrispondente: E = hn, dove h è la costante di Planck
e n la frequenza di
radiazione. Secondo la teoria formulata da Einstein, incidendo sulla
superficie di un corpo metallico, i fotoni cedono la propria energia agli
elettroni del conduttore, provocandone l’estrazione. Ogni elettrone acquista
un’energia cinetica K = 0,5 mu2, dove m è la massa dell’elettrone
e u la sua velocità.
Questa energia è pari a K = hn – F. (2) F rappresenta il potenziale di estrazione del metallo, ovvero l’energia
che deve essere ceduta all’elettrone per svincolarlo dalla forza
elettrostatica dei nuclei atomici che lo trattiene all’interno del metallo
stesso. Si capisce dunque che l’elettrone può essere estratto solo se la
radiazione incidente ha una frequenza pari o superiore a ncr
= F/h: l’energia del fotone in eccesso rispetto al potenziale di
estrazione viene trasferita all’elettrone sotto forma di energia cinetica. È
interessante notare che l’eq. (2) può essere utilizzata per ricavare il
valore della costante di Plank. Si può infatti ripetere l’esperimento due
volte, utilizzando radiazioni di frequenze note diverse n1 e n2, e misurare nei due
casi le energie cinetiche degli elettroni, K1 e K2.
In base all’eq. (2) si ottiene pertanto h = (K1 – K2)/(n1 – n2). Secondo Einstein, dunque, l’energia dell’elettrone liberato
dipende solo dall’energia del fotone, mentre l’intensità della radiazione è
direttamente correlata al numero di fotoni trasportati dalla radiazione e
pertanto può influire sul numero di elettroni estratti dal metallo, ma non
sulla loro energia. Lo scienziato tedesco riuscì così a spiegare tutti i
fatti sperimentali concernenti l’effetto fotoelettrico e gli fu conferito per
questo il premio Nobel nel 1921. |